Protein & Cell封面文章 | 高绍荣/高亚威团队报道m6A识别蛋白YTHDC1调控LINE1染色质脚手架功能
N6-甲基腺嘌呤(N6-methyladenosine, m6A)是真核生物RNA上含量最为丰富的转录后修饰,具有添加和擦除可逆的特征,已被视为重要的RNA层级表观遗传调控而得到广泛研究。近年来,重复序列(repeat)尤其是逆转录转座子(retrotransposon)在调控早期胚胎发育、多能干细胞特性中的功能受到越来越多的关注,虽然已有研究证明了m6A通过促进repeat RNA的降解来调控染色质状态和转录活性[1, 2],但m6A在一些功能性染色质相连RNA(chromatin-associated RNA, caRNA)的反式作用(trans-acting)机制中扮演了怎样的角色尚不明晰。
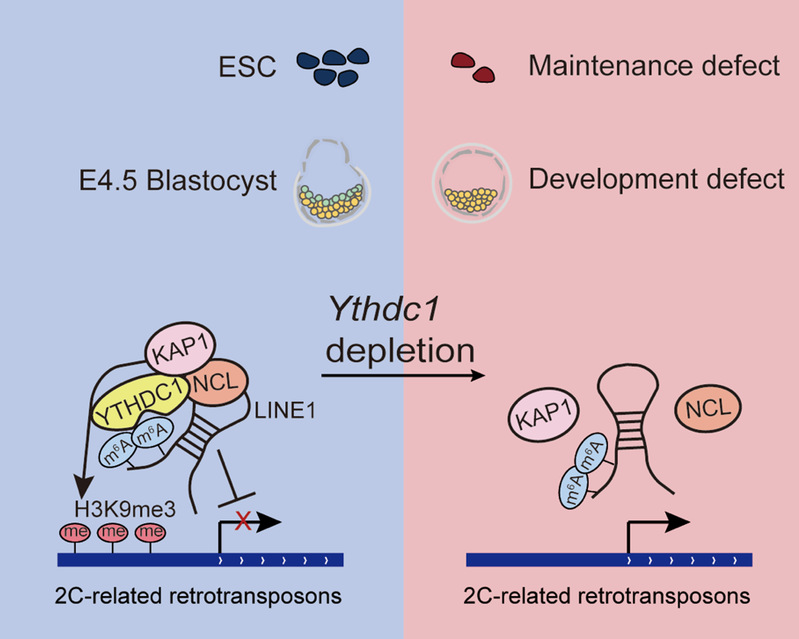
2021年4月22日,3344体育官方入口高绍荣/高亚威团队联合南京医科大学沈彬课题组于Protein & Cell在线发表了题为Nuclear m6A reader YTHDC1 regulates the scaffold function of LINE1 RNA in mouse ESCs and early embryos的研究论文,该研究入选Protein & Cell最新一期的杂志封面(June, 2021, Volume 12, Issue 6, Pages 437-513)。这项工作揭示了细胞核内的m6A识别蛋白YTHDC1在小鼠胚胎干细胞维持和早期胚胎发育中的重要作用,YTHDC1通过结合LINE1(long interspersed nuclear element-1)caRNA上的m6A修饰,促进NCL-KAP1蛋白招募到LINE1调控复合物中,从而保障二细胞(2-cell, 2C)相关逆转录转座子上的H3K9me3建立和转录抑制。

该文作者首先发现Ythdc1对于小鼠胚胎干细胞的自我更新、克隆形成至关重要,且这种作用高度依赖于YTHDC1蛋白识别m6A的能力。深入分析显示, LINE1 RNA上同时有着高度富集的YTHDC1结合及m6A修饰,之前研究已经证明YTHDC1通过识别LINE1 caRNA的m6A修饰来促进RNA降解,且这类m6A由甲基转移酶METTL3建立[1],然而本文作者发现LINE1 caRNA上的一些m6A可能并非依赖于METTL3写入,而这些METTL3非敏感型m6A虽然也能被YTHDC1识别,其存在却并未促进RNA降解。值得注意的是,LINE1 RNA敲降引发的细胞增殖障碍和转录组缺陷[3]同样出现在Ythdc1敲除ESC中,尤其是2C相关基因和逆转座子的上调以及rRNA的下调,而这些表型并未出现在Mettl3敲除ESC中,这说明LINE1 caRNA上的METTL3非敏感型m6A在被YTHDC1识别后很可能影响了LINE1调控染色质状态的脚手架(scaffold)功能。进一步研究发现,YTHDC1与LINE1脚手架复合物中的调控因子NCL-KAP1均存在蛋白间相互作用,而Ythdc1的缺失减弱了NCL对LINE1 RNA的结合,并抑制了KAP1在LINE1复合物靶点上的招募,造成KAP1介导的H3K9me3建立障碍,使得包括2C相关逆转录转座子在内的位点转录去抑制化。该研究首次证明m6A参与了LINE1 RNA对染色质状态的调控,其中YTHDC1作为m6A识别蛋白,促进了RNA和染色质之间的交互作用(cross-talk)。这项工作也提示我们可能存在更多的RNA转录后修饰调控caRNA反式功能的机制,为后续caRNA调控转录活性和染色质开放程度的研究提供了新的思路。
3344体育官方入口直博生陈川和3344体育官方入口附属第一妇婴保健院辅助生殖医学科刘文强研究员为本文的共同第一作者。3344体育官方入口高绍荣教授、高亚威教授及南京医科大学沈彬教授为本文的共同通讯作者。该工作得到了科技部重点研发计划、国家自然科学基金委、上海市科委等项目的支持。
[1] Liu J, Dou X, Chen C, et al., N (6)-methyladenosine of chromosome-associated regulatory RNA regulates chromatin state and transcription. Science, 2020, 367 (6477): 580-586
[2] Chelmicki T, Roger E, Teissandier A, et al., m(6)A RNA methylation regulates the fate of endogenous retroviruses. Nature, 2021, 591 (7849): 312-316
[3] Percharde M, Lin C J, Yin Y, et al., A LINE1-Nucleolin Partnership Regulates Early Development and ESC Identity. Cell, 2018, 174 (2): 391-405 e19
Copyright© 2011-2015 3344体育官方入口 - 3344体育网平台
地址:上海市四平路1239号 电话:021-65981041 传真:65981041


