Nature Communications | 刘默芳/丁德强/王鑫课题组合作揭示小鼠精子发生中MIWI-piRNA复合物在生殖颗粒中的转运机制
生殖颗粒是特异性存在于动物生殖细胞中的无膜细胞器,与多种RNA生成和代谢过程相关。在哺乳动物生殖细胞中,研究最为广泛的生殖颗粒为线粒体簇间的intermitochondrial cement(IMC)和细胞核周的chromatoid body(CB)[1]。研究表明IMC和CB与piRNA的生成以及功能发挥密切相关。piRNA(PIWI interacting RNA)是一种在生殖细胞中高表达的小非编码RNA,与PIWI蛋白形成复合物,通过抑制转座子以及调控功能基因的表达参与配子发生[2]。小鼠生殖细胞中表达三个PIWI蛋白:MILI、MIWI2和MIWI[3]。其中,MIWI在初级精母细胞中开始表达,被TDRKH蛋白募集到IMC中参与piRNA生成。在减数分裂后的圆形精子细胞中,MIWI-piRNA复合物定位于CB中,调节精子形成过程。但是,MIWI在雄性生殖细胞中从IMC转移到CB的机制仍是piRNA研究领域尚未解决的问题。
2024年3月,中科院分子细胞科学卓越创新中心刘默芳研究员、3344体育官方入口丁德强教授和国科大杭州高等研究院王鑫副研究员合作在Nature Communications上在线发表题为 “piRNA loading triggers MIWI translocation from the intermitochondrial cement to chromatoid body during mouse spermatogenesis” 的研究论文。该研究发现MIWI蛋白结合piRNA后可以促进其在小鼠生殖细胞生殖颗粒中的转运,并且这种转运过程是小鼠精子发生正常进行所必需的。

之前的研究表明MIWI蛋白在初级精母细胞中表达后被线粒体膜蛋白TDRKH募集到IMC中[4]。在本项工作中,研究人员首先探讨了MIWI蛋白如何离开IMC。研究人员构建了两种MIWI蛋白结合piRNA缺陷的突变小鼠(MiwiYY/YY和MiwiYK/YK)来研究MIWI蛋白结合piRNA的能力在精子发生中的生理功能。在MiwiYY/YY和MiwiYK/YK小鼠中,缺失piRNA结合能力的MIWI蛋白被滞留在IMC中,无法转运到CB。进一步研究发现MIWI蛋白结合piRNA可以促进MIWI与TDRKH解离,从而允许MIWI从IMC离开。
那么MIWI离开IMC后又是如何进入CB的?研究人员利用MiwiYY/YY、MiwiYK/YK和Tdrd6-/-小鼠研究发现,MIWI与TDRKH解离会暴露其N端的精氨酸残基,经PRMT5(蛋白精氨酸甲基转移酶)甲基化修饰后,被TDRD6识别结合,最终被招募到CB中执行MIWI-piRNA的生物学功能。进一步研究发现MIWI-piRNA复合物转运缺陷会导致MIWI蛋白降解,最终导致小鼠雄性不育。
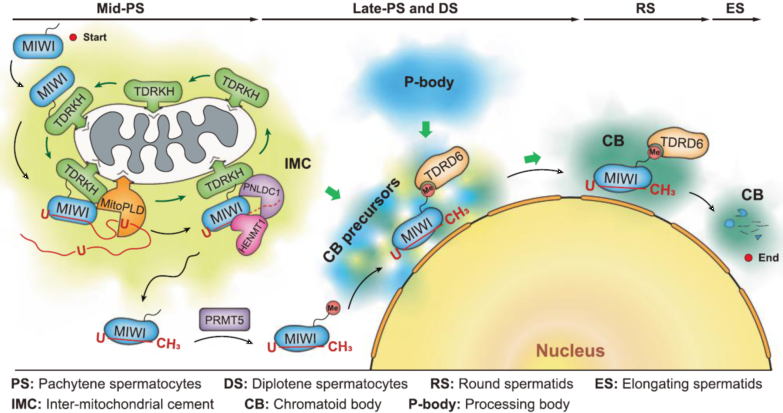
基于以上研究结果,作者提出了MIWI蛋白在小鼠精子发生过程中转运的机制模型:MIWI在粗线期中期的精母细胞中表达,其未甲基化的N端与TDRKH互作而被招募到IMC中参与piRNA的加工。MIWI蛋白与piRNA形成复合物会诱导MIWI的构象发生变化,进而减弱其与TDRKH的相互作用,导致MIWI-piRNA复合物从IMC被释放出来。离开IMC的MIWI蛋白在细胞质中被精氨酸甲基化修饰,从而增强了MIWI与TDRD6的相互作用。最终TDRD6募集MIWI-piRNA复合物进入CB中。总的来说,本文的研究揭示了MIWI与piRNA的结合是如何指导MIWI从IMC转运到CB的分子机制,并且证明了该机制在精子发生中的生物学功能,为男性不育症的检测和治疗提供了理论依据和潜在的靶点。
国科大杭州高等研究院生命学院博士研究生魏欢、3344体育官方入口博士研究生高洁、中科院分子细胞科学卓越创新中心林迪航博士以及3344体育官方入口耿睿嵘硕士为该论文共同第一作者。刘默芳研究员、丁德强教授以及王鑫副研究员为该论文的共同通讯作者。该项工作还得到了中科院分子细胞科学卓越创新中心李劲松研究员和美国密歇根州立大学的Chen Chen教授的大力支持和帮助。本研究得到了国家科技部、国家自然基金委以及上海市科委项目的资助。
参考文献
[1] Lehtiniemi T, Kotaja N. Germ granule-mediated RNA regulation in male germ cells. Reproduction: The official journal of the Society for the Study of Fertility, 2018(2).
[2] Czech B, Marzia.Munafò, Ciabrelli F, et al. piRNA-Guided Genome Defense: From Biogenesis to Silencing. Annual review of genetics, 2018, 52: 131-157.
[3] Deng W, Lin H. miwi, a murine homolog of piwi, encodes a cytoplasmic protein essential for spermatogenesis. Developmental Cell, 2002, 2(6): 819-830.
[4] Deqiang D, Jiali L, Kunzhe D, et al. Mitochondrial membrane-based initial separation of MIWI and MILI functions during pachytene piRNA biogenesis. Nuclc Acids Research, 2019(5): 2594-2608.
3344体育官方入口丁德强教授课题组长期招聘博士后,同时欢迎感兴趣的硕士研究生、博士研究生报考。课题组介绍3344体育官方入口生命学院官网---师资队伍---教授---丁德强。有意者请发邮件至dingdeqiang@tongji.edu.cn。
Copyright© 2011-2015 3344体育官方入口 - 3344体育网平台
地址:上海市四平路1239号 电话:021-65981041 传真:65981041


