Genes & Development|高亚威/张勇/高绍荣团队揭示CTCF在小鼠早期胚胎结合位点动态变化的内在机制
CTCF是一种在哺乳动物中高度保守的DNA结合蛋白,最早作为染色质绝缘子结合蛋白被报道,随后被发现对于染色质高级结构的调控起到至关重要的作用,参与转录激活/抑制、基因印记、X染色体失活等重要事件的调节[1]。CTCF通过识别特定的基序结合到染色质上并作为锚点起到固定染色质环的作用,是构建染色质三维结构的基础[2]。过往的研究发现在小鼠胚胎发育早期,染色质的高级结构在囊胚时期的建立完成伴随着第一次细胞命运决定的发生[3],并参与细胞从全能性向多能性以及后续分化的调控。CTCF的缺失会导致囊胚发育的异常和胚胎的死亡[4, 5]。但是,胚胎早期CTCF结合数据的缺失使得对CTCF在早期胚胎发育过程中作用的研究陷入瓶颈。
2024年3月13日,Genes & Development杂志在线发表了来自3344体育官方入口高亚威/张勇/高绍荣教授团队题为“ADNP modulates SINE B2-derived CTCF-binding sites during blastocyst formation in mice”的研究论文。该研究在小鼠中产生了从配子到囊胚过程中CTCF结合位点的动态图谱,发现了一批衍生出卵裂期特有的CTCF结合位点(cleavage-specific CTCF binding sites, cs-CBSs),探究了cs-CBS产生和消失的内在机制,揭示了其在细胞从全能性向多能性转换这一过程中的潜在作用。

CTCF对于基因组的识别被认为与结合位点的基序与染色质表观修饰状态有关,CTCF结合后会在周围形成周期性的核小体分布。高绍荣/张勇/高亚威团队在此前的合作工作利用低起始量的微球菌核酸酶高通量测序(ULI-MNase-seq),首次检测了小鼠受精后12h内雌雄原核连续时间点的核小体排布模式建立过程,并发现CTCF在受精后3-6小时就已经开始在父源和母源基因组上实现锚定[6],提示CTCF可能作为胚胎早期染色质调控的重要基础元件发挥作用。为解析植入前胚胎中CTCF建立动态的检测,合作团队利用核酸酶靶向切割和释放(cleavage under target and release using nuclease,CUT&RUN)技术,获取了从配子到囊胚过程多个时间点的CTCF结合位点数据,并结合同阶段的核小体排布数据以及已发表的表观数据展开系统研究。团队确认了CTCF结合位点在减数分裂中消失并在合子基因组之前重新结合的现象,并且发现CTCF基序是CTCF结合位点重新建立主导因素。随后,研究人员将研究重点放在了第一次细胞命运决定前后,发现了一批在分化后的内细胞团和滋养外胚层中均消失的位点,将其定义为卵裂期特异的CTCF结合位点(cs-CBS)(图1A)。总结现有发表数据,他们发现相较于r-CBS, cs-CBS在胚胎干细胞中相对各组织器官中具有更高CTCF信号,在各种成体组织中,cs-CBS丢失的CTCF信号不会再恢复(图1B),提示其可能与细胞多能性状态存在关联。进一步分析发现接近80%的cs-CBS由啮齿类特异的重复序列家族SINE B2衍生而来(图1C),并且在第一次细胞命运决定前后,cs-CBS上的激活型H3K4me3修饰显著丢失,抑制型的H3K9me3修饰显著升高,并伴随了结合位点转座子表达活性的显著下降。
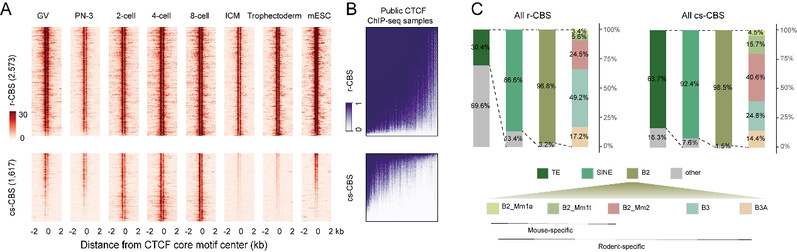
图1. CTCF结合位点的动态与SINE B2衍生的卵裂期特异的CTCF结合位点
在哺乳动物中转座子(Transposable elements,TEs)被发现占据了近一半的基因组序列,并呈现高度的物种特异性。根据转座插入基因组的方式不同,转座子主要分为逆转座子和DNA转座子,逆转座子可以分为SINE(short interspersed nuclear elements,SINEs)、LINE(long interspersed nuclear elements,LINEs)和LTR(long terminal repeats,LTRs)。转座子序列中往往存在大量的转录因子结合位点。在小鼠基因组中,约28% 的CTCF结合位点存在于转座子序列中,在小鼠胚胎干细胞中的研究显示,神经保护蛋白ADNP在SINE B2衍生的CTCF结合位点上同CTCF存在竞争性抑制的关系[7]。通过分析已发表的ADNP结合位点数据,研究人员确认了cs-CBS富集于胚胎干细胞的ADNP结合区域,提示胚胎发育中cs-CBS可能同样受到ADNP蛋白的调节。随后他们利用Crisper-Cas9技术在受精卵中敲除Adnp对于胚胎发育和CTCF结合以及组蛋白修饰等展开检测。他们发现Adnp的敲除会导致囊胚发育异常,内细胞团和滋养外胚层细胞数量的减少,并在着床后的胚胎中引发转录组缺陷与细胞凋亡增强,胚胎在E7.5大量死亡。同时他们也发现在敲除后囊胚的cs-CBS上,可以观察到CTCF结合信号的恢复、H3K9me3修饰信号的下降、H3K4me3修饰信号的轻微回升以及结合位点上SINE B2表达的回升。这些结果都表明ADNP蛋白参与了小鼠囊胚分化过程中CTCF在cs-CBS上的结合活性与表观修饰改变。
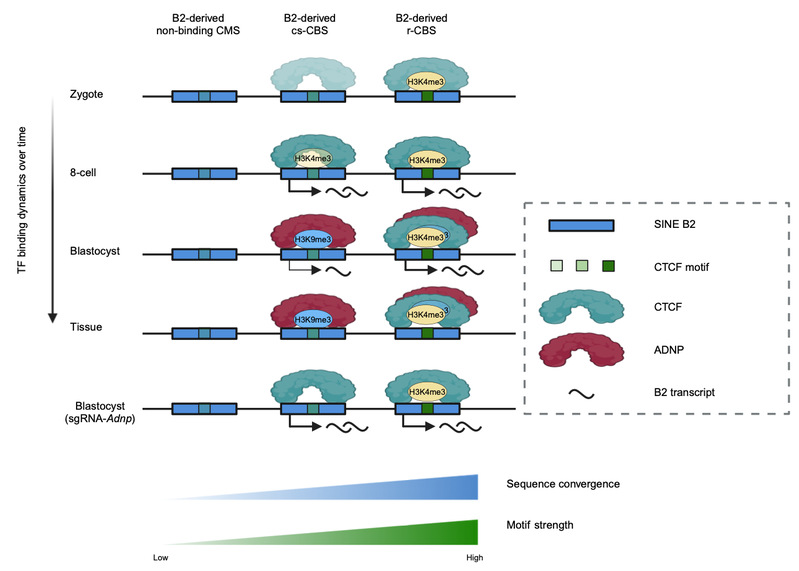
图2. SINE B2衍生的不同CTCF基序序列在发育过程中的变化情况
进一步的,研究人员发现相较于小鼠胚胎干细胞,cs-CBS在二细胞样细胞(two-cell like cells, 2CLC)中具有更高的CTCF结合信号。此外,在小鼠胚胎干细胞通过敲降Adnp可以得到更高比例的MERVL激活型2CLC,提示ADNP对于cs-CBS活性的调控可能与细胞全能性的退出与逆转座子抑制等过程相关。作者还通过对于重复序列家族SINE B2衍生出的的不同类型CTCF结合位点进行比较,提出了大部分由重复序列衍生的转录因子基序进化过程中是一种中型突变这一观点。
综上所述,该研究首次绘制了小鼠植入前胚胎的CTCF结合动态,发现了物种特异性转座子介导的卵裂期特异的CTCF结合特征,发现了囊胚分化过程中ADNP介导的CTCF结合限制。此研究不仅首次解析了CTCF在早期胚胎中的动态模式与调控模型,也进一步扩展了转座子参与胚胎发育的染色质重塑和转录活性调控的可能路径,在理解转座子调控发育与基因组进化方面具有重要意义。3344体育官方入口王文博士、高睿副教授、直博生杨东旭、直博生马明莉为本文的共同第一作者,3344体育官方入口高亚威教授、张勇教授、高绍荣院士为本文的共同通讯作者。
[1] CHOUDHARY M N K, QUAID K, XING X, et al. Widespread contribution of transposable elements to the rewiring of mammalian 3D genomes [J]. Nat Commun, 2023, 14(1): 634.
[2] HASHIMOTO H, WANG D, HORTON J R, et al. Structural Basis for the Versatile and Methylation-Dependent Binding of CTCF to DNA [J]. Mol Cell, 2017, 66(5): 711-20 e3.
[3] DU Z, ZHENG H, HUANG B, et al. Allelic reprogramming of 3D chromatin architecture during early mammalian development [J]. Nature, 2017, 547(7662): 232-5.
[4] ANDREU M J, ALVAREZ-FRANCO A, PORTELA M, et al. Establishment of 3D chromatin structure after fertilization and the metabolic switch at the morula-to-blastocyst transition require CTCF [J]. Cell Rep, 2022, 41(3): 111501.
[5] CHEN X, KE Y, WU K, et al. Key role for CTCF in establishing chromatin structure in human embryos [J]. Nature, 2019, 576(7786): 306-10.
[6] WANG C, CHEN C, LIU X, et al. Dynamic nucleosome organization after fertilization reveals regulatory factors for mouse zygotic genome activation [J]. Cell Res, 2022, 32(9): 801-13.
[7] KAAIJ L J T, MOHN F, VAN DER WEIDE R H, et al. The ChAHP Complex Counteracts Chromatin Looping at CTCF Sites that Emerged from SINE Expansions in Mouse [J]. Cell, 2019, 178(6): 1437-51 e14.
Copyright© 2011-2015 3344体育官方入口 - 3344体育网平台
地址:上海市四平路1239号 电话:021-65981041 传真:65981041


